Как вылечить хронический лимфолейкоз

Хронический лимфоцитарный лейкоз (ХЛЛ) — это злокачественное заболевание кроветворной ткани, характеризующееся опухолевой трансформацией одного клона лимфоцитов с последующей экспансией им костного мозга, крови, лимфатических узлов и внутренних органов. Злокачественные клетки замещают нормальные, что приводит к дисфункции пораженных органов, расстройствам кровообращения и иммунной защиты.
Одним из первых лабораторных признаков лимфолейкоза является кратное увеличение количества лейкоцитов в периферической крови.
Содержание:
- Причины возникновения ХЛЛ
- Симптомы ХЛЛ
- Диагностика ХЛЛ
- Стадии хронического лимфоцитарного лейкоза
- Лечение хронического лимфоцитарного лейкоза
Причины развития хронического лимфолейкоза
К возможным этиологическим факторам развития хронического лимфолейкоза относят:
- хромосомные мутации
- наследственная предрасположенность
- вирусные инфекции

По мнению ряда ученых, длительная стимуляция иммунной системы человека (например, при частых инфекциях) может приводить к генетическим поломкам и опухолевому перерождению лимфоцитов, образованию клона лейкемических клеток и возникновению ХЛЛ.
Прямой причинной связи между воздействием канцерогенов, ионизирующего излучения и возникновением ХЛЛ не установлено.
Механизм развития хронического лимфолейкоза заключается в преобразовании лимфоцитов в опухолевые клетки и их размножении, что приводит к угнетению нормального кроветворения, развитию анемии и тромбоцитопении.
Симптомы хронического лимфолейкоза
В начальной стадии ХЛЛ пациенты не предъявляют жалоб, их общее состояние удовлетворительное. У некоторых могут проявляться такие неспецифические симптомы как: сильная потливость, быстрая утомляемость, слабость, частые простуды. На данном этапе ХЛЛ выявляется, как правило, случайно на профилактическом осмотре или при обращении к доктору по поводу другого заболевания. Заболевание проявляется абсолютным лимфоцитозом в общем анализе крови и увеличением периферических групп лимфатических узлов (шейных, подмышечные, паховые). Увеличенные лимфоузлы при ХЛЛ пальпаторно мягко — эластичные, безболезненные, не спаяны с окружающими тканями, кожа над ними не изменена.
При медленном течении начальная стадия может длиться несколько лет, при прогрессирующем течении наблюдается быстрое ухудшение общего состояния, значительное увеличение лимфоузлов и селезенки.
Для развернутой стадии ХЛЛ характерна выраженность симптомов. К основным клиническим проявлениям относят:
- синдром интоксикации: выраженная слабость, быстрая утомляемость, снижение работоспособности, резкое снижение массы тела, значительная потливость в ночное время, необъяснимое повышение температуры тела;
- прогрессирующая лимфоаденопатия: увеличиваются практически все группы лимфатических узлов. На ощупь они мягко-эластичные, безболезненные, не спаяны с окружающими тканями, могут сливаться в конгломераты;
- инфильтрация опухолевыми клетками всех органов и систем со снижением их функции.
При этом наблюдаются:
- увеличение селезенки;
- увеличение печени, с чем связаны синдромы портальной гипертензии (расширение вен пищевода, скопление свободной жидкости в брюшной полости, печеночная недостаточность) и холестатической желтухи (боль в правом подреберье, тошнота, окрашивание кожи и склер в желтый цвет, кожный зуд, обесцвечивание кала, потемнение мочи);
- язвы ЖКТ, синдром мальабсорбции (нарушение всасывания в кишечнике, сопровождающееся болями в животе, диареей), диспепсические нарушения (тошнота, вздутие, чувство тяжести), как следствие инфильтрации ЖКТ;
- частые пневмонии и другие инфекции дыхательных путей, дыхательная недостаточность, вследствие накопления опухолевых клеток в легких.
В общем анализе крови — лейкоцитоз (50-200*109/л), лимфоцитоз (до 100*109/л или 80-90 % в лейкоцитарной формуле), анемия и тромбоцитопения, увеличение СОЭ, клеток Боткина — Гумпрехта (разрушенные лимфоциты).
Терминальная стадия ХЛЛ характеризуется:
- резким значительным ухудшением общего состояния;
- длительной высокой температурой тела;
- истощением;
- тяжелыми генерализованными инфекциями (стафилококковой, стрептококковой, герпетической, туберкулезом и др.);
- тяжелой почечной недостаточностью (характеризуется олигоанурией, повышением в крови мочевины и креатинина);
- выраженной анемией;
- выраженная тромбоцитопения;
- геморрагический синдром;
- в связи с инфильтрацией мозговых оболочек опухолевыми клетками возможно развитие нейролейкемии, проявляющейся сильной головной болью, рвотой, парезами и параличами, развитием менингеальных симптомов;
- инфильтрация спинномозговых корешков сопровождается интенсивными стреляющими «корешковыми» болями;
- возможно развитие тяжелой кардиомиопатии, проявляющейся прогрессирующей сердечной недостаточностью и нарушениями ритма сердца.
Диагностика хронического лимфолейкоза
Диагностика хронического лимфоцитарного лейкоза включает в себя сбор анамнеза и уточнение жалоб у пациента, общий осмотр, который заключается в прощупывании периферических лимфатических узлов, печени и селезенки.
Лабораторные методы исследования ХЛЛ
- Общий анализ крови с лейкоцитарной формулой (оценка количества эритроцитов, лейкоцитов, тромбоцитов, СОЭ, определение наличия в мазке крови клеток Боткина — Гумпрехта). Основной диагностический критерий абсолютный лимфоцитоз (более 5*109/л).
- Общий анализ мочи.
- Биохимический анализ крови (оценка уровня общего белка и белковых фракций, билирубина, креатинина, мочевины, ЛДГ, железа, щелочной фосфатазы, глюкозы).
- Исследование коагулограммы.
- Иммунологический анализ крови — оценка количества и функций иммунных клеток крови, присутствие в ней антител (определение количества В — и Т-лимфоцитов, субпопуляций Т-лимфоцитов, иммуноглобулинов, ревматоидного фактора, циркулирующих иммунных комплексов).
- Иммунофенотипирование лимфоцитов — исследование лимфоцитов с помощью специальных маркеров, которое позволяет определить их принадлежность к определенному виду.
- Цитологическое исследование костного мозга с миелограммой.
- Цитогенетическое исследование.
- ПЦР-диагностика вирусных инфекций.
Инструментальные методы исследования ХЛЛ
- Рентгенография органов грудной клетки.
- Ультразвуковое исследование периферических лимфатических узлов и органов брюшной полости, почек.
- Компьютерная томография органов грудной клетки, брюшной полости, малого таза.
- ЭКГ и эхокардиография.
- Эндоскопические исследования (фиброгастродуоденоскопия и колоноскопия).
Также проводятся трепанобиопсия костного мозга и биопсия лимфатических узлов с последующим гистологическим и иммуногистохимическим исследованиями.
Стадии хронического лимфолейкоза
Существует две системы стадирования ХЛЛ, в основы которых положен единый принцип: учет массы опухоли (лимфоцитоз), размеры лимфатических узлов, степень увеличения печени и селезенки, наличие или отсутствие анемии и тромбоцитопении. Совокупность данных фактор влияет на продолжительность жизни и предопределяет прогноз.
Стадии ХЛЛ по европейской классификации Binet
| Стадия | Характеристики | Прогноз | ||
| Анемия HGB | Тромбоциты PLT | Увеличение лимфоузлов | ||
| A | >100 г/л | >100×109 /л | в 1-2 областях | хороший |
| B | >100 г/л | >100×109 /л | в 3 и более областях | промежуточный 7+ лет |
| C | >100 г/л | >100×109 /л | любое количество зон | плохой |
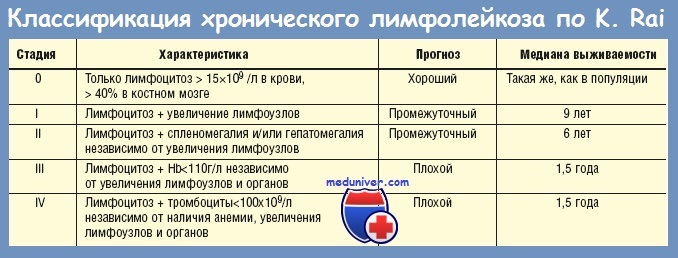
Стадии ХЛЛ по американской классификации RAI
| Стадия | Характеристики | Прогноз | |||
| Лимфоцитоз | Анемия | Тромбоциты PLT | Лимфоузлы увеличены | ||
| 0 | >15×109 /л в костном мозге: >40% | нет | норма ≥150 x109 /л | нет | хороший |
| I | есть | нет | норма/около нормы | да | относительно хороший |
| II | есть | нет | норма/около нормы | да/нет + сплено/гематомегалия | промежуточный 6+ лет |
| III | есть | да | норма/около нормы | да/нет | плохой |
| IV | есть | да/нет | <110 x109 /л | да/нет | плохой |
Лечение хронического лимфолейкоза
Течение ХЛЛ неоднородно, поэтому подход к лечению в каждом случае индивидуален и учитывает особенности состояния пациента. Может наблюдаться волнообразный характер течения ХЛЛ с периодами накопления и спонтанной регрессии опухолевого объема. Лечение ХЛЛ подразделяется на специфическую терапию, направленную на подавление клеток опухоли, и симптоматическую терапию.
Специфическая терапия
- Химиотерапия — лечение лекарственными препаратами, подавляющими рост клеток опухоли. Является основным методом лечения.
- Кортикостероидные препараты. Применяются при выраженной анемии и тромбоцитопении.
- Таргерная терапия — терапия направленного действия с использованием моноклональных антител. Позволяет уничтожать непосредственно опухолевые клетки, не повреждая здоровые ткани организма.
- Лучевая терапия. Используется для облегчения состояния у пациентов со значительным увеличением лимфатических узлов, селезенки и печени. Облучению подвергаются вовлеченные зоны.
- Спленэктомия. Показана в случаях тяжелых анемии и тромбоцитопении, не поддающихся медикаментозному лечению; частых инфарктах селезенки, значительного увеличения селезенки, которое не поддается лучевой и цитостатической терапии и вызывает сдавление органов брюшной полости.
Показаниями к назначению специфической терапии являются:
- один или более симптомов интоксикации: снижение массы тела более 10% в течение 6 месяцев; необъяснимые подъемы
- температуры тела более 38 более двух недель; ночная потливость в течение 1 месяца; выраженная слабость;
- нарастающая анемия иили тромбоцитопения;
- значительное увеличение размеров селезенки (более 6 см ниже реберной дуги);
- нарастающая лимфаденопатия;
- время удвоения лимфоцитов в течение менее 6 месяцев.
Симптоматическая и поддерживающая терапия
- Переливание эритроцитарной массы или применение эритропоэтина при анемии.
- Переливание тромбоцитарной массы при тромбоцитопении.
- Применение антибактериальных, противовирусных и противогрибковых препаратов при присоединении инфекций и др.
Хронический лимфоцитарный лейкоз в настоящее время является неизлечимым заболеванием. Однако своевременное и адекватно назначенное лечение позволяет добиться длительных ремиссий, значительно увеличить продолжительность жизни и улучшить её качество.
Источник
Современное лечение хронического лимфолейкоза — химиотерапия
Основным методом лечения хронического лимфолейкоза является химиотерапия. Верификация диагноза хронического лимфолейкоза не всегда является показанием для проведения противоопухолевой терапии. В ряде случаев (обычно в дебюте заболевания) оправдана выжидательная тактика, так как доказано, что раннее начало лечения не увеличивает выживаемость больных хроническим лимфолейкозом.
Показания к началу химиотерапии:
1) синдром опухолевой интоксикации (проливные ночные поты, лихорадка выше 38 °С, снижение массы тела);
2) анемия или тромбоцитопения, обусловленные опухолевой инфильтрацией костного мозга;
3) аутоиммунная гемолитическая анемия или тромбоцитопения (при отсутствии ответа на глюкокортикостероиды);
4) выраженная лимфоаденопатия и/или спленомегалия с компрессией органов и тканей с нарушением их функций;
5) время удвоения абсолютного лимфоцитоза в периферической крови меньше 12 месяцев;
6) гипогаммаглобулинемия, сопровождающаяся рецидивирующими инфекционными осложнениями;
7) массивная лимфоцитарная инфильтрация костного мозга;
8) лейкоцитоз больше 150 • 109/л;
9) стадия III—IV по классификации К. Rai.
Основным препаратом для лечения хронического лимфолейкоза является хлорбутин (хлорамбуцил, лейкеран). Существует 2 основных режима назначения препарата:
1) малые дозы (0,07 мг/кг массы тела через день в течение 14 дней; курс повторяется каждые 28 дней);
2) большие дозы (0,7 мг/кг один раз в неделю).
Эффект достигается у 2/3 больных, побочное действие практически отсутствует. После получения ответа на лечение проводится поддерживающая терапия в дозе 10-15 мг 1-3 раза в неделю.
Применение хлорбутина позволяет быстро снизить количество лейкоцитов, однако уменьшение лимфатических узлов и селезенки достигается не всегда. Поэтому при преобладании в клинической картине лимфоаденопатии и спленомегалии с умеренным лейкоцитозом может использоваться комбинированная терапия хлорбутином и преднизолоном (преднизолон 30-70 мг в сутки + хлорбутин 10-20 мг в сутки) курсами по 5-14 дней с перерывами 2-4 недели.
При непереносимости хлорбутина, резистентности к препарату, а также у лиц моложе 60 лет можно применять циклофосфан в дозе 2-3 мг/кг в сутки ежедневно внутрь или 1000 мг внутривенно каждые 2 недели. Эффективность препарата сравнима с хлорбутином, однако возможны побочные эффекты (диспепсия, геморрагический цистит).
Преднизолон в дозе 30-60 мг/м2 внутрь ежедневно назначается при аутоиммунной гемолитической анемии или тромбоцитопении. После достижения эффекта доза глюкокортикостероидов постепенно уменьшается до полной отмены препарата.
При неэффективности монотерапии и прогрессировании заболевания (а в ряде случаев — и в качестве индукционного курса) возможно проведение полихимиотерапии по программам СОР (циклофосфан, винкристин, преднизолон) или CHOP (СОР+адриабластин). У пожилых пациентов с сопутствующими заболеваниями сердечно-сосудистой системы доза адриабластина редуцируется (программа мини-СНОР).
Непосредственный эффект комбинированного лечения хороший, однако достоверного увеличения медианы выживаемости по сравнению с пациентами, получавшими монохимиотерапию, не отмечено. Следует иметь в виду также более выраженную токсичность программ полихимиотерапии по сравнению с монотерапией.
Стандартные режимы монохимиотерапии и полихимиотерапия увеличивают продолжительность жизни больных в среднем на 2-3 года.
В последние годы в клиническую практику внедрено новое поколение цитостатических препаратов для лечения хронического лимфолейкоза — аналоги пуриновых нук-леозидов (флударабин, пентостатин, кладрибин).
Наибольшее распространение получил флударабин, который может использоваться как при резистентности к другим цитостатикам (эффективность 50-60%, частота полных ремиссий 25%), так и для первичной терапии (эффективность 80%, частота полных ремиссий 40-50%). Флударабин назначается внутривенно (болюсом или капельно) ежедневно в дозе 25 мг/м2 в течение 5 дней. В среднем необходимо проведение 6 курсов лечения с 28-дневными интервалами между ними.
Основным побочным эффектом является выраженная миелосупрессия с возможным развитием инфекционных осложнений, реже отмечаются аутоиммунная гемолитическая анемия и нейротоксичность. В целом флударабин переносится хорошо и в настоящее время рассматривается как наиболее эффективный препарат для лечения больных хроническим лимфолейкозом как в виде монотерапии, так и в сочетании с другими препаратами (чаще всего с циклофосфаном, митоксантроном и ритуксимабом).
Последние несколько лет характеризуются активным внедрением для лечения хронического лимфолейкоза моноклональных антител: анти-CD20 (Mabthera, Rituximab) и анти-CD52 (Campath-1, Alemtuzumab). Мабтера в настоящее время используется в комбинации с флударабином и алкилирующими агентами при проведении химиотерапии первой линии. При проведении химиотерапии второй линии применяются комбинация мабтеры, пентостатина и циклофосфана и другие режимы.
Анти-CD52 (Campath-1, Alemtuzumab) рекомендуется для проведения химиотерапии второй линии в виде монотерапии или в сочетании с другими цитостатиками.

Современные химиотерапевтические подходы к лечению хронического лимфолейкоза:
I. Химиотерапия 1-й линии:
— Флударабин ± ритуксимаб
— Хлорбутин ± преднизолон
— Циклофосфан ± преднизолон
— СОР (циклофосфан. винкристин, преднизолон)
— FC (флударабин, циклофосфан) ± ритуксимаб
II. Химиотерапия 2-й линии:
— Алемтузумаб
— PC (пентостатин, циклофосфан) ± ритуксимаб
— Полихимиотерапия ± ритуксимаб или алемтузумаб
В последние годы при хроническом лимфолейкозе изучается эффективность трансплантации аллогенных гемопоэтических стволовых клеток и биологических методов лечения.
Трансплантация аллогенных гемопоэтических стволовых клеток используется у больных моложе 55 лет при наличии неблагоприятных прогностических факторов (в частности, высокого уровня ZAP-70). Этот метод лечения используется редко, так как большинство пациентов старше 60 лет и имеют большое количество сопутствующих заболеваний.
После трансплантации достоверно увеличивается общая выживаемость, однако это нивелируется высокой смертностью, обусловленной лечением. При внедрении немиелоаблативных режимов кондиционирования количество больных хроническим лимфолейкозом, которым показана трансплантация, может существенно увеличиться, а совершенствование метода позволит уменьшить количество осложнений.
В ряде случаев у больных хроническим лимфолейкозом могут применяться паллиативные методы лечения (лучевая терапия, спленэктомия, лейкоцитаферез).
Лучевая терапия используется при наличии выраженной спленомегалии или конгломерата лимфатических узлов с признаками компрессии окружающих органов.
Необходимость в спленэктомии у больных хроническим лимфолейкозом возникает редко. Показания к спленэктомии:
а) аутоиммунная гемолитическая анемия, резистентная к терапии глюкокортикостероидами и цитостатическими препаратами;
б) выраженная спленомегалия, не поддающаяся консервативным методам лечения, в том числе лучевой терапии.
Лейкоцитаферез может использоваться для профилактики и лечения лейкостаза у больных с гиперлейкоцитозом, при резистентном к терапии хронического лимфолейкоза или при наличии противопоказаний к химиотерапии.
Лечение осложнений хронического лимфолейкоза (инфекционных, аутоиммунных) проводится по общим принципам онкогематологии.
К новым методам лечения, эффективность которых изучается у больных хроническим лимфолейкозом, относятся:
1) антисмысловые олигонуклеотиды (в частности, направленные против BCL-2);
2) генная терапия, направленная на изменение иммунофенотипа хронического лимфолейкоза;
3) комбинированная терапия мабтерой и ингибиторами ZAP-70;
4) моноклональные антитела к детерминантам опухолевых клеток (HLA-DR, CD40 и др.).
— Также рекомендуем «Прогноз хронического лимфолейкоза — эффективность лечения»
Оглавление темы «Хронический лимфолейкоз»:
- Хронический лимфолейкоз — причины, механизмы развития
- Клиника хронического лимфолейкоза — проявления
- Лабораторная диагностика хронического лимфолейкоза — анализы
- Классификация хронического лимфолейкоза К. Rai и J. Binet
- Современное лечение хронического лимфолейкоза — химиотерапия
- Прогноз хронического лимфолейкоза — эффективность лечения
- Волосатоклеточный лейкоз — клиника, диагностика, лечение
- Пролимфоцитарный лейкоз — клиника, диагностика, лечение
- Хронические Т-клеточные лейкозы — Т-клеточная лейкемия, лимфома кожи, синдром Сезари
- Иммуносекретирующие опухоли — причины, механизмы развития
Источник